Stwardnienie zanikowe boczne (ALS) to jedna z najcięższych chorób neurodegeneracyjnych, która nie tylko wpływa na funkcje motoryczne, ale również prowadzi do szeregu złożonych problemów biologicznych, w tym zaburzeń homeostazy żelaza. Żelazo odgrywa kluczową rolę w wielu procesach życiowych, jednak jego nadmiar może okazać się toksyczny, co stawia pacjentów w trudnej sytuacji. U osób chorych na ALS często obserwuje się zwiększone stężenie żelaza. Warto zauważyć, że w połączeniu z innymi mechanizmami, a nie tylko nadmierną akumulacją, może to prowadzić do poważnych problemów dla systemu nerwowego.
- Stwardnienie zanikowe boczne (ALS) jest ciężką chorobą neurodegeneracyjną, która prowadzi do zaburzeń homeostazy żelaza.
- Żelazo odgrywa kluczową rolę w procesach życiowych, jednak jego nadmiar może być toksyczny dla pacjentów z ALS.
- Stres oksydacyjny jest istotnym czynnikiem degeneracji neuronów ruchowych, związanym z nadmiernym gromadzeniem żelaza.
- Transport żelaza do ośrodkowego układu nerwowego jest regulowany przez mechanizmy komórkowe, w tym interakcje między neuronami a komórkami glejowymi.
- Hepcydyna jest hormonem regulującym metabolizm żelaza, którego działanie jest kluczowe w kontekście chorób neurodegeneracyjnych, w tym ALS.
- Astrocyty i oligodendrocyty mają kluczowe znaczenie w utrzymaniu homeostazy żelaza w mózgu oraz w transporcie tego pierwiastka do neuronów.
- Badania nad zaburzeniami homeostazy żelaza mogą prowadzić do nowych strategii terapeutycznych, takich jak stosowanie antyoksydantów i chelatatorów żelaza.
- Zrozumienie roli komórek glejowych oraz mechanizmów regulacji hepcydyny w OUN może otworzyć nowe możliwości w leczeniu chorób neurodegeneracyjnych.
Badania jednoznacznie ukazują, że stres oksydacyjny odgrywa kluczową rolę w degeneracji neuronów ruchowych, co wiąże się z nadmiernym gromadzeniem żelaza. Na poziomie komórkowym istnieją mechanizmy sprzyjające zwiększonemu pobieraniu żelaza przez neurony, co, w efekcie, prowadzi do powstawania toksycznych form tego pierwiastka. Taka sytuacja pogarsza stan pacjentów z ALS, ponieważ te zaburzenia dodatkowo intensyfikują objawy choroby. W rezultacie, naruszenie równowagi żelaza wpływa zarówno na funkcjonowanie neuronów, jak i na ogólny stan zdrowia chorych.
Stres oksydacyjny w stwardnieniu zanikowym bocznym jako skutek zaburzeń żelaza
W kontekście ALS, szczególne znaczenie nabiera badanie mechanizmów regulujących transport żelaza do ośrodkowego układu nerwowego. Zrozumienie dynamiki tego transportu przez bariery krew-mózg oraz krew-płyn mózgowo-rdzeniowy dostarcza kluczowych informacji o ryzyku rozwoju choroby. W rzeczywistości, interakcje między różnymi typami komórek, takimi jak neurony i komórki glejowe, mają istotny wpływ na homeostazę żelaza. Ich zaburzenia mogą prowadzić do zwiększenia tzw. labilnego żelaza, co wywołuje poważne konsekwencje dla funkcji neuronów.
Rozwój nowych terapii w ALS staje się coraz bardziej obiecujący. Dzięki badaniom nad zaburzeniami metabolizmu żelaza, możemy liczyć na przyszłe innowacje w leczeniu tej skomplikowanej choroby.
Badania nad zaburzeniami homeostazy żelaza w ALS dostarczają cennych wskazówek dotyczących nowych strategii terapeutycznych. Antyoksydanty oraz chelatatory żelaza, które zmniejszają stężenie tego pierwiastka w ośrodkowym układzie nerwowym, mogą stać się obiecującymi elementami w walce z tą chorobą. Nieustalne dążenie do zrozumienia molekularnych mechanizmów metabolizmu żelaza ma niezwykle dużą wagę, ponieważ może otworzyć drzwi do nowatorskich podejść terapeutycznych, mających na celu poprawę jakości życia pacjentów z ALS. Jednak wciąż wiele pytań pozostaje bez odpowiedzi, dlatego badania w tym obszarze są kluczowe dla dalszego zrozumienia niuansów choroby oraz rozwoju skutecznych terapii.
| Aspekt | Informacje |
|---|---|
| Choroba | Stwardnienie zanikowe boczne (ALS) |
| Rola żelaza | Kluczowy element w procesach życiowych |
| Problematyka | Zaburzenia homeostazy żelaza i toksyczność nadmiaru |
| Objawy | Zwiększone stężenie żelaza u pacjentów |
| Stres oksydacyjny | Kluczowy czynnik w degeneracji neuronów ruchowych |
| Mechanizmy komórkowe | Zwiększone pobieranie żelaza przez neurony |
| Konsekwencje dla zdrowia | Naruszenie równowagi żelaza i pogorszenie stanu pacjentów |
| Badania nad transportem | Istotne dla zrozumienia rozwoju choroby |
| Interakcje komórkowe | Wpływ neuronów i komórek glejowych na homeostazę żelaza |
| Nowe terapie | Antyoksydanty i chelatatory żelaza jako obiecujące opcje leczenia |
| Waga badań | Zrozumienie molekularnych mechanizmów metabolizmu żelaza |
Mechanizmy transportu żelaza w ośrodkowym układzie nerwowym: jak działa bariera krew-mózg
W poniższej liście przedstawiam szczegółowe kroki dotyczące mechanizmów transportu żelaza w ośrodkowym układzie nerwowym oraz działania bariery krew-mózg. Każdy punkt dokładnie opisuje etap tego złożonego procesu, podkreślając jednocześnie kluczowe elementy oraz mechanizmy regulacji.
- Przekroczenie bariery krew-mózg (BBB): Żelazo, aby dotrzeć do ośrodkowego układu nerwowego (OUN), musi przejść przez barierę, znaną jako BBB. Ta bariera składa się z ściśle przylegających komórek śródbłonka naczyń włosowatych, które tworzą nieprzepuszczalną struktury. Kluczowe elementy tego procesu to komórki perycytów, które wzmacniają BBB oraz astrocyty, które wspomagają transport żelaza za pomocą swoich wypustek (tzw. stóp ssących), które łączą się z komórkami śródbłonka. Dzięki temu możliwa staje się regulacja transportu substancji, w tym żelaza, z krwi do mózgu.
- Mechanizm transportu za pomocą transferyny: W organizmie żelazo transportowane jest głównie przez białko zwane transferyną (Tf). To białko wiąże dwa jony żelaza, działając jako kluczowy nośnik podczas procesu endocytozy. Na powierzchni komórek śródbłonka naczyń włosowatych BBB znajdują się receptory transferynowe (TfR1), które umożliwiają wychwytywanie żelaza. Po związaniu z Tf, żelazo trafia do wnętrza komórek, a następnie uwalnia się z endosomu w wyniku redukcji jonów Fe3+ do Fe2+.
- Uwolnienie żelaza do cytoplazmy: Po uwolnieniu żelaza z transferyny, jony Fe2+ trafiają do cytoplazmy komórki śródbłonkowej za pośrednictwem białka DMT1 (dwuwartościowy transporter metali). W cytoplazmie żelazo może być magazynowane w ferrytynie lub wykorzystywane do produkcji hemoglobiny oraz centrów żelazowo-siarkowych, co jest niezwykle ważne dla funkcji metabolicznych komórek OUN.
- Transport ferrytyny przez błonę podstawną BBB: Część uwolnionego żelaza, zwłaszcza jego nadmiar, gromadzi się w formie ferrytyny, która następnie przemieszcza się przez błonę podstawną BBB. To umożliwia dystrybucję żelaza do przestrzeni międzykomórkowej w OUN, co przyczynia się do zachowania równowagi metabolicznej.
- Regulacja hepcydyną: Hepcydyna, peptyd syntetyzowany głównie w wątrobie, odgrywa kluczową rolę w regulacji metabolizmu żelaza. Choć najczęściej znana z działania w obrębie układu krążenia, jej ekspresja również zaobserwowana została w OUN, co sugeruje, że może wpływać na transport żelaza w mózgu poprzez oddziaływanie na ferroportynę znajdującą się na błonie komórek śródbłonkowych. Ostatecznie, modulacja hepcydyny wpływa na dostępność żelaza i może mieć kluczowe znaczenie w kontekście chorób neurodegeneracyjnych, takich jak ALS.
Rola hepcydyny w regulacji metabolizmu żelaza: znaczenie dla zdrowia mózgu
Hepcydyna odgrywa kluczową rolę w regulacji metabolizmu żelaza w organizmie. Jej główną funkcją jest kontrolowanie stężenia żelaza we krwi, co realizuje poprzez modulację działania ferroportyny, białka transportującego żelazo z komórek do krwi. W momencie, gdy w organizmie pojawia się wysoka koncentracja hepcydyny, hormon ten łączy się z ferroportyną, a to prowadzi do jej degradacji. W efekcie, dostępność żelaza z makrofagów i enterocytów maleje. Mechanizm ten staje się szczególnie istotny w kontekście stanów zapalnych, które mogą negatywnie wpływać na zdrowie mózgu. Kiedy dochodzi do zaburzenia działania hepcydyny, może wystąpić nadmierna akumulacja żelaza, co obserwuje się w licznych chorobach neurodegeneracyjnych, takich jak stwardnienie zanikowe boczne (ALS).
Wszystkie te zjawiska sprawiają, że hepcydyna ma kluczowe znaczenie w utrzymaniu odpowiedniej równowagi żelaza w ośrodkowym układzie nerwowym (OUN). Odkrycie jej ekspresji w różnych typach komórek mózgowych, w tym astrocytach i oligodendrocytach, sugeruje, że lokalna regulacja hepcydyny może znacząco wpływać na transport oraz wykorzystanie żelaza w mózgu. U pacjentów z ALS zaobserwowano zmiany w metabolizmie żelaza, co potwierdza hipotezę o potencjalnym uczestnictwie hepcydyny w patogenezie tych chorób. Odkrycia te fascynują, ponieważ tworzą pomost między globalną homeostazą żelaza a lokalnym metabolizmem w OUN.
Hepcydyna reguluje transport żelaza i jego akumulację w mózgu
W badaniach pokazano, że w OUN stężenia hepcydyny mogą zmieniać się w odpowiedzi na rozmaite czynniki, takie jak stres oksydacyjny czy zapalenie. Wzrost produkcji hepcydyny może skutkować ograniczeniem dostępności żelaza, co dodatkowo wpływa na funkcje neuronów, w tym na ich zdolność do regeneracji oraz przetrwania. Interesujące jest również to, że hepcydyna działa nie tylko ogólnoustrojowo, ale także lokalnie w tkankach mózgowych, co może być kluczowe w zrozumieniu, jak niewłaściwa regulacja tego hormonu oddziałuje na stan zdrowia mózgu. W przypadku nadmiaru żelaza w neuronach mózg staje się bardziej podatny na uszkodzenia, co wiąże się z rozwojem degeneracyjnych schorzeń neurologicznych.
Podsumowując, rola hepcydyny w regulacji metabolizmu żelaza w OUN ma ogromne znaczenie. Zrozumienie mechanizmów wpływających na jej ekspresję oraz działanie w kontekście mózgu może otworzyć nowe ścieżki terapeutyczne w walce z chorobami neurodegeneracyjnymi. W szczególności, możemy lepiej pojąć, dlaczego hepcydyna staje się kluczowym graczem w utrzymaniu zdrowia mózgu oraz jak można ją skutecznie wykorzystać w leczeniu stanów patologicznych związanych z akumulacją żelaza.
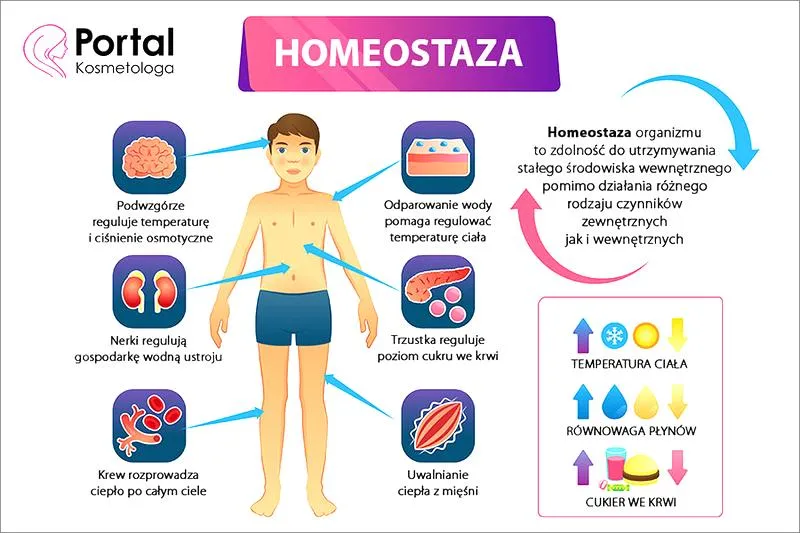
Poniżej przedstawiono czynniki wpływające na stężenia hepcydyny w OUN:
- Stres oksydacyjny
- Stan zapalny
- Poziom żelaza w organizmie
- Obecność bakterii lub toksyn
Ciekawostką jest, że hepcydyna nie tylko reguluje poziom żelaza w organizmie, ale również może być wykorzystywana jako potencjalny biomarker w diagnostyce chorób neurodegeneracyjnych, co otwiera możliwości wczesnego wykrywania i leczenia takich schorzeń.
Astrocyty i oligodendrocyty: kluczowe komórki w homeostazie żelaza w OUN
Astrocyty oraz oligodendrocyty pełnią kluczowe funkcje w regulacji homeostazy żelaza w ośrodkowym układzie nerwowym (OUN). Astrocyty, będące największymi komórkami glejowymi, odgrywają istotną rolę w tworzeniu bariery krew-mózg, a także w utrzymywaniu równowagi składników odżywczych, w tym żelaza, w mózgu. Oligodendrocyty natomiast wspierają mielinizację neuronów i zapewniają im wsparcie metaboliczne. Ich zaangażowanie w metabolizm żelaza odgrywa szczególnie ważną rolę, ponieważ umożliwia dostarczenie tego pierwiastka do neuronów oraz jego magazynowanie w odpowiednich formach, co jest kluczowe dla funkcji nerwowej.
Molekularne mechanizmy przekraczania bariery krew-mózg są skomplikowane i do tej pory wciąż pozostają w granicach naukowej zagadki. Jednym z głównych białek transportujących żelazo jest transferyna (Tf), której interakcja z receptorami komórkowymi pozwala na dostęp do żelaza w OUN. Zgodnie z wynikami badań, astrocyty syntetyzują apotransferynę, co umożliwia efektywne regulowanie poziomu żelaza w przestrzeni międzykomórkowej. W kontekście patologii, takich jak stwardnienie zanikowe boczne (ALS), nadmiar żelaza w OUN prowadzi do stresu oksydacyjnego, co podkreśla znaczenie astrocytów i oligodendrocytów w utrzymaniu równowagi żelaza, a także ich potencjalny wpływ na degenerację neuronów.
Rola astrocytów i oligodendrocytów w transportowaniu żelaza do neuronów

Zaburzenia w metabolizmie żelaza w OUN mogą prowadzić do poważnych konsekwencji, dlatego walka z tymi problemami wymaga zaangażowania badań nad różnymi komórkami glejowymi. U pacjentów z ALS oraz w badaniach na modelach zwierzęcych, naukowcy obserwują podwyższone stężenie ferrytyny i zwiększoną akumulację żelaza w komórkach glejowych. To sugeruje, że oligodendrocyty mogą szczególnie odczuwać skutki nadmiaru żelaza. Z kolei wzrost ekspresji receptorów dla transferyny oraz zwiększona ilość białek magazynujących żelazo mogą wskazywać na rosnące zapotrzebowanie na ten pierwiastek lub jego nadprodukcję przy jednoczesnym osłabieniu mechanizmów usuwania. Takie zmiany negatywnie wpływają nie tylko na oligodendrocyty, ale także na neurony, co sprawia, że zrozumienie roli tych komórek w homeostazie żelaza staje się kluczowe dla badań nad terapiami neurodegeneracyjnymi.
Homeostaza żelaza w OUN przypomina balet, w którym każda komórka odgrywa istotną rolę w złożonej choreografii. Chociaż astrocyty i oligodendrocyty często pozostają w cieniu neuronów, ich wpływ na metabolizm żelaza zyskuje coraz większe uznanie. Badania nad ich rolą mogą przynieść nowe informacje, które zrewolucjonizują podejście do terapii chorób neurodegeneracyjnych. Kluczowe może okazać się zrozumienie, jak różne komórki glejowe współpracują w regulacji i transporcie żelaza. Takie podejście może okazać się przełomowe w walce z chorobami takimi jak ALS oraz innymi, w których zaburzenia homeostazy żelaza mają znaczący wpływ na przebieg schorzeń.
Źródła:
- https://phmd.hirszfeld.pl/zaburzenie-homeostazy-zelaza-w-stwardnieniu-zanikowym-bocznym/